Новые бактерии в олиготрофной среде
Все мы знаем о средах обитания, в которых очень мало питательных веществ для поддержания жизни, ранее я писал о проекте «искусственной корки» на основе цианобактерий, который разрабатывается китайскими учеными, пустыня - это как раз один из примеров такой среды.
Ученые называют такие среды обитания олиготрофными.
К ним относятся также, например, выщелоченные почвы, ледниковые и полярные льды, пещеры (это все естественные среды обитания) и созданные человеком олиготрофные среды, такие как чистые помещения, в которых регулярно проводятся всевозможные дезинфекции.
В NASA возник прецедент, который выводит на новый уровень вопрос выживаемости бактерий.
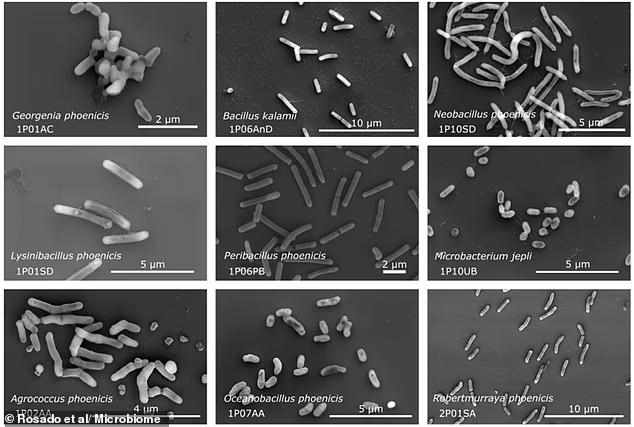
Считается, что стерильные помещения со строгим контролем, где строятся и тестируются космические аппараты и чувствительные приборы - это одни из самых стерильных мест на Земле, но недавно учёные обнаружили в них десятки новых видов бактерий.
Эти объекты были предназначены для предотвращения любых форм заражения и предотвращения попадания нежелательных микробов на другие планеты, поэтому эксперты были ошеломлены, когда обнаружили 26 разных видов крошечных микроорганизмов — все ранее неизвестные бактериальные виды — в чистых помещениях Космического центра Кеннеди во Флориде.
Несмотря на сложный комплекс мер, таких как фильтрация воздуха, строгое регулирование температуры и влажности, а также использование очень агрессивных химических моющих средств, эти микробы каким-то образом сумели выжить.
И оказывается, у них есть гены, которые помогают им противостоять воздействию радиации и даже восстанавливать собственную ДНК.
"Это был настоящий момент истины, когда мы поняли, что пора подвергнуть сомнению все наши предыдущие познания о выживаемости микроорганизмов.
Хотя таких микробов было относительно мало, они сохранялись долгое время и в нескольких очень чистых и стерильных помещениях." - заявил Александр Росадо, профессор бионаук в Научно-технологическом университете имени короля Абдаллы (KAUST) в Саудовской Аравии в интервью Live Science
Выявление этих необычно выносливых организмов и изучение их стратегий выживания имеют значение, отмечают исследователи, поскольку любой микроб, способный пройти через стандартные чистые помещения, может также обойти меры планетарной защиты, направленные на предотвращение заражения земными микроорганизмами других обитаемых планет.
Они также играют ключевую роль в защите Земли от возможных инопланетных автостопщиков в возвращённых образцах.
Ученые также отметили, что помимо освоения космоса, эти микробы обладают огромным потенциалом для биотехнологий, поскольку их устойчивость к радиации и химическим стрессорам может стимулировать инновации в медицине, фармацевтике и пищевой промышленности.
Показывай это видео жене, когда хочешь выпить
Добавляем каплю виски в раствор с бактериями
Микробиом и рак. Бактерия из ЖКТ рептилий уничтожила раковые опухоли у мышей
В материалах часто ссылаюсь на микробиом, как на эдакий универсальный нормализатор и точку приложения усилий для продления жизни. И, само собой, для повышения продуктивности. И вот тому очередной доказательство. Внутривенно введенная бактерия, взятая из микробиома рептилий, привела к подавлению раковых опухолей у мышей.
Рептилии, млекопитающие, рак
Бактерия из кишечника японских древесных лягушек проявила «невероятно мощные» противоопухолевые свойства при внутривенном введении. Результат инъекции превзошел существующие стандартные методы лечения, открыв путь к совершенно новому подходу в лечении рака.
Исследователи из Японского института передовых наук и технологий (JAIST) проявляли большой интерес к микробиому амфибий и рептилий. Ключевые факторы:
Спонтанные опухоли у рептилий встречаются крайне редко. А если и встречаются, то их причина или в отравлении веществами или в заданных лабораторных условиях. Другими словами, рак который вызван напрямую внешними факторами окружающей среды.
У рептилий внушительная продолжительность жизни относительно их размеров.
Они естественным образом переносят сильный клеточный стресс при метаморфозах и регенерации.
А также живут в среде богатой патогенами. Причем наличие патогенов – это краеугольный фактор, повышающий риск развития рака.
Исследователи предположили, что защита от рака вполне может поддерживаться микробиомом, а не одними лишь клетками организма. Тем более что сам микробиом влияет на широкий спектр процессов организма. И отчасти это проявляется при голодании, с целью подавить рак.
Потенциальная бактерия, защищающая от рака
Ученые выделили 45 штаммов бактерий из древесных лягушек, японских огненнобрюхих тритонов (Cynops pyrrhogaster) и японских травяных ящериц (Takydromus tachydromoides). Перебирая эти штаммы, удалось сузить потенциальный список до девяти бактерий. Причем все эти девять бактерий поддерживали противоопухолевый эффект. Но наиболее сильный ответ показала бактерия Ewingella americana, обнаруженная у древесных лягушек.
Ewingella americana продемонстрировала невероятно мощную цитотоксическую активность, вместе с избирательной способностью к поражению опухолей. Исследования показали, что E. americana действует через два механизма: прямое уничтожение опухолевых клеток и мощная активация иммунитета хозяина. Благодаря чему опухоль подвергается атаке от Т-клеток, нейтрофилов и В-клеток.
Лечение с помощью E. americana значительно превзошло стандартные методы терапии, включая антитела к PD-L1 и доксорубицин, в исследованиях регрессии опухолей.
Исследование противораковой бактерии
Исследовательская группа ввела мышам с колоректальным раком единоразово инъекцию E. americana внутривенно. Эта инъекция полностью уничтожила опухоли у всех обработанных животных. Более того, эффект был не только быстрым, но и, по-видимому, обеспечивал длительную защиту. Когда мышей позже повторно подвергли воздействию раковых клеток, ни у одной из них не развились новые опухоли. То есть, лечение вызвало долговременную иммунную память.
Бактерия E. americana использует двухступенчатый механизм для борьбы с раковыми клетками. Бактерия сама по себе адаптирована к среде с низким содержанием кислорода, идеально размножаясь внутри твердых опухолей. Всего за 24 часа численность бактерий выросла примерно в 3000 раз. При этом она не распространилась на другие здоровые органы или ткани. А также бактерия напрямую уничтожает раковые клетки благодаря токсинам, которые она выделяет внутри опухоли.
Одновременно с этим, само бактериальное вторжение вызвало естественный иммунный ответ. Вскоре после инъекции опухоли наполнились иммунными клетками – особенно нейтрофилами, Т- и В-клетками. И это при параллельном росте воспалительных сигнальных молекул. Совокупный эффект привел к массовой гибели опухолевых клеток, вызванной как прямым воздействием чужеродных кишечных бактерий, так и собственной иммунной системой хозяина.
Насколько безопасно уничтожать рак чужими бактериями?
Результаты свидетельствуют о том, что кишечный микробиом низших позвоночных содержит множество неидентифицированных видов бактерий, обладающих исключительным терапевтическим потенциалом. Исследование закладывает основу для разработки природных, непатогенных бактериальных терапевтических средств и подчеркивает критическую важность биоразнообразия для совершенствования стратегий лечения рака.
Важно отметить, что этот механизм высоко специфичен по отношению к раку. Бактерии E. americana прикрепляются только к опухолевой среде. Исследователи полагают, что такая избирательность обусловлена сочетанием факторов, уникальных для опухолей: дефицит кислорода, повышенная проницаемость кровеносных сосудов, измененный метаболизмом и локально подавленная иммунная защита. Все это вместе и позволяет бактериальной колонии развиваться там, где она наиболее разрушительна.
Заражение бактериями ради лечения рака. Насколько оправдано?
Исследования показали, что E. americana быстро выводилась из кровотока, и не оставляла следов уже через 24 часа. Максимум, вызывая лишь кратковременные воспалительные эффекты, которые проходили в течение 72 часов.
В течение двух месяцев наблюдений за мышами, получавшими лечение, не наблюдалось никаких признаков повреждения органов или хронической токсичности. При этом сама бактерия чувствительна к антибиотикам. То есть, всегда можно вмешаться, если на фоне лечения начнутся проблемы.
Всесторонняя оценка безопасности на мышиных моделях показала, что штамм E. americana, выделенный из кишечника, минимально патогенный и не оказывает значительного неблагоприятного воздействия в терапевтически эффективных дозах. Это выгодно отличается от генетически модифицированных бактериальных препаратов.
Из материалов исследования.
Когда можно будет использовать бактерии рептилий для лечения рака у людей?
Само собой, эти результаты предварительны и экспериментальны, тем более что получены на мышах. И хоть опухоли человека и мышей схожи через молекулярные маркеры, включая множество общих генов, существуют и различия. Самое главное – естественные иммунные реакции и работа иммунной системы в целом.
Тем не менее, это многообещающий новый метод для противораковой терапии с использованием естественных бактерий. Причем метод, который потенциально способен полностью уничтожить раковые опухоли как явление.
Потенциал исследования
Сейчас ученые изучают потенциал бактерий при раке молочной железы, раке поджелудочной железы, меланоме и других злокачественных новообразованиях, а также уточнят методы доставки и дозировки.
Также исследуется потенциал бактерий как дополнительной терапии наряду с существующими методами иммунотерапии и химиотерапии.
Традиционно, больше статей о грани, где технологии сливаются с биологией и ведут к сингулярности – читайте в материалах Neural Hack. Подписывайтесь, чтобы не пропускать свежие статьи!
Одобрено два новых антибиотика против гонореи, в том числе устоийчивых штаммов
Гонорея — инфекционное заболевания, вызываемое бактерией Neisseria gonorrhoeae. Передаётся половым путём и является вторым по «популярности» бактериальным половым заболеванием. В мире ежегодно заражается примерно 80 млн. человек.
Особенность данной бактерии в том, что она выработала резистентость практически ко всем видам антибиотиков. Сейчас гонорею лечат с помощью уколов цефтриаксона, и, по сути, это единственный антибиотик, к которому бактерия не обрела устойчивость. Хотя в последнее время стали появляться штаммы Neisseria gonorrhoeae, которых и цефтриаксон плохо берёт.
В общем, ещё несколько лет — и здравствуй, 18-й и 19-й века, когда бактериальные ЗППП были огромной проблемой. К счастью, эти славные новые старые времена откладываютс.
FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) на днях одобрило целых два новых антибиотика, предназначенных для лечения гонореи. Впервые за 30 лет, и действительно с новым механизмом действия, к которым бактерии ещё не выработала резистентность.
Это Blujepa (gepotidacin) (все совпадения случайны!) и Nuzolvence (zoliflodacin). Оба препарата нацелены на ингибирования ДНК-гиразы — специфического для одноклеточных фермента, участвующего в репликации ДНК.
Blujepa
Это таблетки, предназначенные для приёма 2 раза в день людьми старше 12 лет и весом свыше 45 килограмм. В прошедших клинических испытаниях Blujepa показал эффективность в 93% выздоровивших после 4-10 дней лечения. Стандартная терапия в виде цефтриаксона в уколах и таблетированного азитромицина показала эффективность в 91%.
Кроме неосложнённой гонореи, Blujepa также подходит для лечения других неосложнённых заболеваний мочевыводящих путей у женщин и детей старше 12 лет:
Escherichia coli;
Klebsiella pneumoniae, ;
Citrobacter freundii complex;
Staphylococcus saprophyticus;
Enterococcus faecalis.
Nuzolvence
С этим антибиотиком ещё проще: он представляет собой суспензию, которая разводится в стакане воды. Доза всего одна — выпил, и свободен. Предназначен для лечения людей в возрасте от 12 лет и весом от 35 килограмм. В прошедших клинических испытаниях Nuzolvence показал эффективность в 91% против стандартного лечения (цефтриаксон в уколах и таблетированный азитромцин) в 96%.
Увы, потенциальные побочки у Nuzolvence тоже достаточно серьёзны. На животных моделях были зафиксированы следующие негативные эффекты:
Снижением фертильности у мужчин;
Вред для плода, вплоть до выкидыша;
Аллергические реакции.
Это не значит, что побочки обязательно будут у людей, но опасаться стоит.
Плюсы-минусы
Основной плюс новых препаратов — в новом механизме действия. Резистентности к нему пока нет, так что несколько лет человечество на Blujep’e/Nuzolvence ещё протянет. Возможно, даже с десяток, учитывая, что новые лекарства вмешиваются в ключевой механизм функционирования бактерий. Это спасение для тех, у кого бактерии выработали резистентность или есть реакция на препараты первой линии.
Дополнительный плюс — в отсутствии укола. За дозой цефтриаксона нужно идти в медцентр/больницу, да и сам по себе он весьма болезненный. С таблетками или суспензией куда проще.
Минусы — в цене и побочках, которые могут оказаться велики. Так что лучше не болеть.
P.S. Ещё у меня есть бессмысленные и беспощадные ТГ-каналы (ну а как без них?):
Вот тут про молекулярную биологию, медицину и новые исследования: https://t.me/nextmedi;
Мой личный, куда сваливается наука и всякое гиковское: https://t.me/deeplabscience.